Autoantikörper-Stufendiagnostik bei Autoimmunerkrankungen
Abbildung 1: Modell der Autoantikörper-Stufendiagnostik bei Verdacht auf eine systemische Autoimmunerkrankung.
Stufe 1 ANA-Screening mittels IFT (multispezifisch) inkl. aktuelle ICAP-Nomenklatur
Stufe 2 ENA-Screen (FEIA) und AMA/ASMA/LKM (IFT)
Stufe 3 AAk-Subtypenbestimmung (monospezifisch)
Testprinzip: grün = IFT; blau = FEIA; orange = Immunoblot (IgG)
NB = Nebenbefund, *diese AAk Subtypen sind im ENA-Profil einzeln enthalten
Stufe 1: Antikörper-Screening mittels IFT – ein multispezifischer Suchtest
Die Stufendiagnostik (s. Abbildung 1) bei Verdacht auf eine systemische Autoimmunerkrankung beginnt mit der Bestimmung von Autoantikörpern (AAk) gegen Zellkerne, auch ANA (antinukleäre Antikörper) genannt. Die AAk Bestimmung gegen intrazelluläre Strukturen (Kern und Zytoplasma) wird mittels indirekter Immunfluoreszenztechnik (IFT) auf Objektträgern mit fixiertem mitotisch aktivem Zellmaterial (HEp-2 Zellen und Primatenleberzellen) durchgeführt. Die Antikörper im Patientenserum binden dabei spezifisch an ihre intrazelluläre Zielstruktur und werden mittels fluoreszenzmarkiertem Anti-human IgG sichtbar gemacht. Bei positivem Test (Titer ≥1:100 Erwachsene;≥1:32 bei Kindern bis 17 Jahre) wird eine Untersuchung mit serieller Verdünnung des Patientenserums (Austitrierung bis Titer 1:10.000) angeschlossen.
Je nach Antigenlokalisation ergibt sich für jeden ANA ein charakteristisches Fluoreszenzmuster, das zusätzlich zum ANA-Titer im Befund angegeben wird. Die Befundung der ANA-Fluoreszenzmuster erfolgt auf Basis der ICAP-Nomenklatur (International consensus on antinuclear antibody patterns) für die Standardisierung und Vergleichbarkeit von ANA-Befunden. Der ICAP-Code unterscheidet 33 ANA-Fluoreszenzmuster AC-1 bis AC-31 + AC-XX; AC-0 bedeutet negativer ANA (Abkürzung AC: anti-cell pattern; ) (s. Abbildungen 2 und 3).

Abbildung 2: Übersicht der HEp-2-Zellmuster gemäß ICAP-Nomenklatur (anti-cell pattern, AC).
Die Klassifikation unterscheidet derzeit über 30 Muster (AC-0 bis AC-31 sowie AC-XX für nicht klassifizierbare Muster).
Bildquelle: , basierend auf ICAP-Richtlinien.
Ein negatives Testergebnis stellt aufgrund der hohen Sensitivität ein nahezu sicheres Ausschlusskriterium für einige Kollagenosen (z.B. SLE und Mischkollagenose/SHARP-Syndrom) dar (hoher negativer prädiktiver Wert). Jedoch sollte trotzdem immer die zusätzliche Bestimmung der SS-A/Ro-Ak erfolgen, da bekannt ist, dass ANA, die sich gegen das Antigen SS-A/Ro richten, im IFT nicht immer erfasst werden (Häufigkeit > 2 %). Hier ist eine spätere Verlaufs-Wiederholung des ANA-Tests empfohlen. ANA kommen nicht nur bei systemischen Autoimmunerkrankungen, z. B. Kollagenosen, wie dem systemischen Lupus erythematodes (SLE) oder Rheumatoider Arthritis (RA), sondern auch bei organspezifischen Autoimmunerkrankungen wie der autoimmunen Hepatitis, bei vielen Infektionserkrankungen sowie ggf. bei gesunden Personen vor.
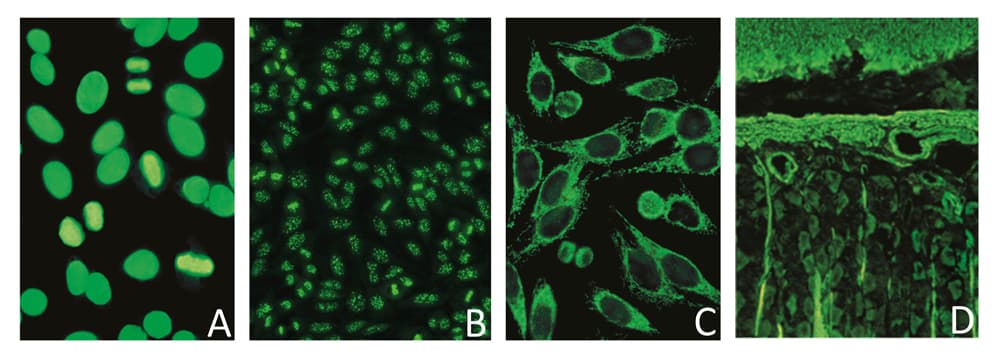
Abbildung 3: Beispiele für positive Fluoreszenzmuster.
A) ANA, homogenes Muster (AC-1); B) ANA, Zentromere (AC-3); C) AMA (AC-21); D) ASMA (AC-15)
Bilderquelle: EUROIMMUN AG
Stufe 2: ENA-Screen (Pool) und AMA, ASMA, LKM:
Positive ANA lassen je nach Art und Titer bestimmte Hinweise auf den/die zugrundeliegenden Autoantikörper bzw. Erkrankung zu. 95-99 % aller Patienten mit systemischem Lupus erythematodes (SLE) und 30 % aller Patienten mit Rheumatoider Arthritis (RA) sind ANA positiv. Die hohe Sensitivität korreliert allerdings mit einer nur geringen Spezifität. Auch bei Gesunden, vor allem bei älteren Patienten (> 60 Jahre) sind niedrigtitrige ANA nachweisbar, allerdings ohne pathologische Relevanz. Sie können jedoch den Beginn oder die Remission einer Kollagenose oder einer autoimmunen Lebererkrankung anzeigen (jährliche Kontrolle!). Bei einem positiven Antikörpernachweis ≥1:1000, sollte in einem zweiten Schritt, je nach Fluoreszenzmuster und diagnostischer Fragestellung, eine weitere gezielte Differenzierung der Subtypen erfolgen:
- Bei einem Kernfluoreszenzmuster und bei möglichen Überlappungen ist die Bestimmung von Antikörpern gegen ENA (extrahierbare nukleäre Antigene) empfohlen. Der ENA-Screen (Pool) mittels Fluoreszenzenzymimmunoassay (FEIA) dient zur qualitativen in vitro Bestimmung von IgG-Antikörpern und stellt eine Hilfe bei der klinischen Diagnose SLE, Mischkollagenose, Sjögren-Syndrom, Sklerodermie und Polymyositis/Dermatomyositis dar. Der ENA-Screen ist ein Gemisch aus den humanen rekombinanten Antigenen U1-snRNP (RNP70, A, C), SS-A/Ro (60 kDa, 52 kDa), SS-B/La, CENP-B, Scl-70, und Jo-1 Proteinen und den synthetischen SmD Peptiden. Bei einem positiven ENA Ergebnis sollte eine Differenzierung der Reaktivität (s. Stufe 3, monospezifischer Test) erfolgen.
- Bei einem homogenen Muster oder bei positiven Chromosomen im Mitosestadium empfiehlt sich zusätzlich die Bestimmung von dsDNA-Antikörpern. Der dsDNA-Antikörper ist ein krankheitsspezifischer Autoantikörper bei SLE und wird mit einer Prävalenz von 70-90 % festgestellt.
- Bei einem rein zytoplasmatischen Fluoreszenzmuster empfiehlt sich die Bestimmung von antimitochondrialen Autoantikörpern (AMA-IFT), AK gegen Leber-Niere-Mikrosomen (LKM-IFT) und Autoantikörpern gegen glatte Muskulatur (ASMA-IFT) sowie Parietalzellen (H+/K+ ATPase und Intrinsic Faktor, FEIA). Diese Autoantikörper-Spezifitäten können auf einem speziellen IFT Organschnitt bestätigt werden.
Stufe 3: monospezifischer Test – Autoantikörper Subtypenbestimmung
Bei einem positiven ENA-Screen sollte in einem dritten Schritt eine entsprechende Differenzierung der Subtypen erfolgen, da diese Autoantikörper eine z.T. deutlich höhere Krankheitsspezifität besitzen (s. Tabelle):
Subtyp | Mögliche Krankheitsassoziation | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| dsDNA-Ak | SLE | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SS-A/Ro-Ak | Sjögren-Syndrom, SLE | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SS-B/La-Ak | Sjögren-Syndrom, SLE | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tabelle 1: Subtypen und mögliche Krankheitsassoziation.
SLE: systemischer Lupus erythematodes,
CREST: Calcinose, Raynaud, Oesophagusdysmotilität, Sklerodaktylie, Teleangiekatsien;
PBC: primäre biliäre Zirrhose
- ENA-Profil (monospezifischer Test mittels FEIA) mit humanen rekombinanten U1-snRNP (RNP70, A, C), SS-A/Ro (60 kDa, 52 kDa), SS-B/La, CENP-B, Scl-70, und Jo-1 Proteinen sowie mit synthetischen SmD Peptiden
- Weitere mögliche AAk-Einzelparameter: RNP70, dsDNA und DFS70. Bestätigung dsDNA mit Crithidien IFT und Farr-RIA.
- Bei einem zytoplasmatischen Fluoreszenzmuster kann eine Subtypenbestimmung der AAk AMA M2-Protein, LKM-1 sowie Parietalzellen (Intrinsic Faktor und H+/K+ ATPase) erfolgen.
- Je nach Fragestellung können hier auch zusätzlich spezielle Immunoblots (z.B. Myositis-/ Sklerodermie-IgG Profile) folgen.
Klinische Relevanz
In verschiedenen retrospektiven und prospektiven Studien für einige AAk konnte zudem gezeigt werden, dass diese Monate bis Jahre vor den klinischen Symptomen der entsprechenden Autoimmunerkrankung bereits nachweisbar sind. Solche Antikörper positive Patienten sollten engmaschig kontrolliert werden, um eine frühzeitige Therapie einleiten zu können.
- Rheumafaktor (RF) und zyklisch citrullinierte Peptide (CCP-Ak) können Jahre vor der Manifestation der Rheumatoide Arthritis nachweisbar sein. Besonders hoch ist das Risiko einer RA-Entwicklung, wenn beide Autoantikörper erhöht auftreten.
- Bei 88 % der SLE-Patienten konnte gezeigt werden, dass mindestens einer der SLE-AAk (ANA, dsDNA, SS-A/Ro, SS-B/La, SmD oder U1-snRNP) bis zu drei Jahren vor der Manifestation bereits nachweisbar ist.